
Edadismo de la industria farmacéutica: el Ministerio de Sanidad responde a la denuncia de 65YMÁS
Defienden que las autoridades competentes velan "porque haya una inclusión adecuada y suficiente"

Edadismo alarmante en la industria farmacéutica: la mayoría de medicamentos no se prueba en mayores
Los sénior, indignados: No probar medicamentos en mayores atenta contra "el derecho a la salud"
Los geriatras denuncian: Las farmacéuticas no prueban medicamentos en mayores porque sale más caro
La infrarrepresentación o exclusión "sistemática" de mayores de 75 años en los ensayos clínicos de la mayoría de vacunas y medicamentos para la diabetes, el cáncer o el colesterol, denunciada por diversos geriatras y representantes de especialidades médicas en este diario, tiene muchas vertientes. Todo apunta que no es solo responsabilidad de la industria farmacéutica, investigadores o pacientes, si no que, según los expertos consultados, también recae sobre los organismos reguladores de medicamentos y vacunas como la Agencia Española de Medicamentos y Productos Sanitarios (@AEMPSGOB), que depende del Ministerio de Sanidad (@sanidadgob).
"Aunque la conciencia sobre incluir pacientes diversos es cada vez mayor, los estudios publicados hasta la actualidad muestran que hay una infrarrepresentación de las personas mayores en los ensayos clínicos de la mayoría de fármacos y vacunas que hay en el mercado, especialmente de mayores de 70 y sobre todo mayores de 80 años, explica José Augusto García Navarro, presidente de la Sociedad Española de Geriatría y Gerontología(@seggeriatria). Además aclara que cuando se les incluye, suele ser en grupos muy pequeños y en individuos que no se parecen a los pacientes reales que van a la consulta, es decir, que están más sanos o tienen una única enfermedad, lo cual no es tan frecuente en muchos mayores entre los que predomina la presencia de 2 a 5 enfermedades de media en cada persona. "Esto complica la administración de cualquier tratamiento a este grupo de edad", añade.
La valoración del Ministerio
De ahí que hemos consultado con el Ministerio que lidera Mónica García en busca de una valoración sobre esta infrarrepresentación de los mayore y si tienen algún plan para combatirlo. Además hemos querido saber qué tienen que decir ante la petición casi unánime por parte de geriatras, asociaciones de mayores, Carlos San Juan y el presidente del Comité Médico de la sección de 65YMÁS, Cuídate+, José Ramón Calvo, , de que sean los agentes reguladores quienes deberían asegurar – a través de una regulación "más estricta"– que se cumpla una representación suficiente de "pacientes reales mayores" en los estudios, teniendo en cuenta tanto a los de mayor edad, como la presencia de más de una enfermedad.
A este respecto, el Ministerio de Sanidad ha explicado a este diario que "en las solicitudes de autorización de ensayos clínicos presentadas en España, los criterios de inclusión y exclusión se evalúan exhaustivamente tanto por el área de ensayos clínicos de la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS) como por los Comités de Ética de la Investigación con Medicamentos (CEIm).

Aseguran que el 80% de los ensayos en España incluyen a mayores de 65 años
No obstante, admiten que "en pacientes de edades avanzadas es más frecuente que haya enfermedades concomitantes que en ocasiones impiden que puedan participar en ciertos ensayos clínicos", uno de las "exclusiones invisibles a las que hacían referencia varios expertos consultados. "La edad media de exclusión en estudios de fracturas eran los 75 años y en aquellos estudios en los que la edad por sí misma no aparecía como criterio de exclusión, se mencionaba el tiempo desde la menopausia, tener deterioro cognitivo o tener problemas de movilidad", según explica la doctora Cristina Alonso Bouzón, geriatra del Servicio Madrileño de Salud centrada en fragilidad y expresidenta de la Sociedad Española de Medicina Geriátrica (@semeg_es).
Sin embargo, desde el Ministerio de Sanidad, en representación también de la Agencia Española de Medicamentos y Productos Sanitarios, defienden que "las autoridades competentes velamos porque haya una inclusión adecuada y suficiente de todos los grupos poblacionales en los ensayos clínicos. Y como prueba de ello, afirman que "en torno al 80% de los ensayos clínicos autorizados en España en los últimos dos años incluyen pacientes mayores de 65 años", pero a cierre de este artículo, aún no nos han facilitado el dato de cuántos mayores de 75 años están incluidos en estos ensayos – grupo poblacional que los geriatras apuntan no solo como infrarrepresentados, sino también como los mayores consumidores de medicamentos–.
En una simple búsqueda en el Registro Español de Ensayos Clínicos, encontramos que en un estudio al azar que entre los criterio de inclusión se especifica ser mayor de 18 años y menor de 75 años (ver imagen). En concreto, se trata de un estudio preclínico sobre la golexanolona y su efecto en pacientes con fatiga y disfunción cognitiva de 2023.
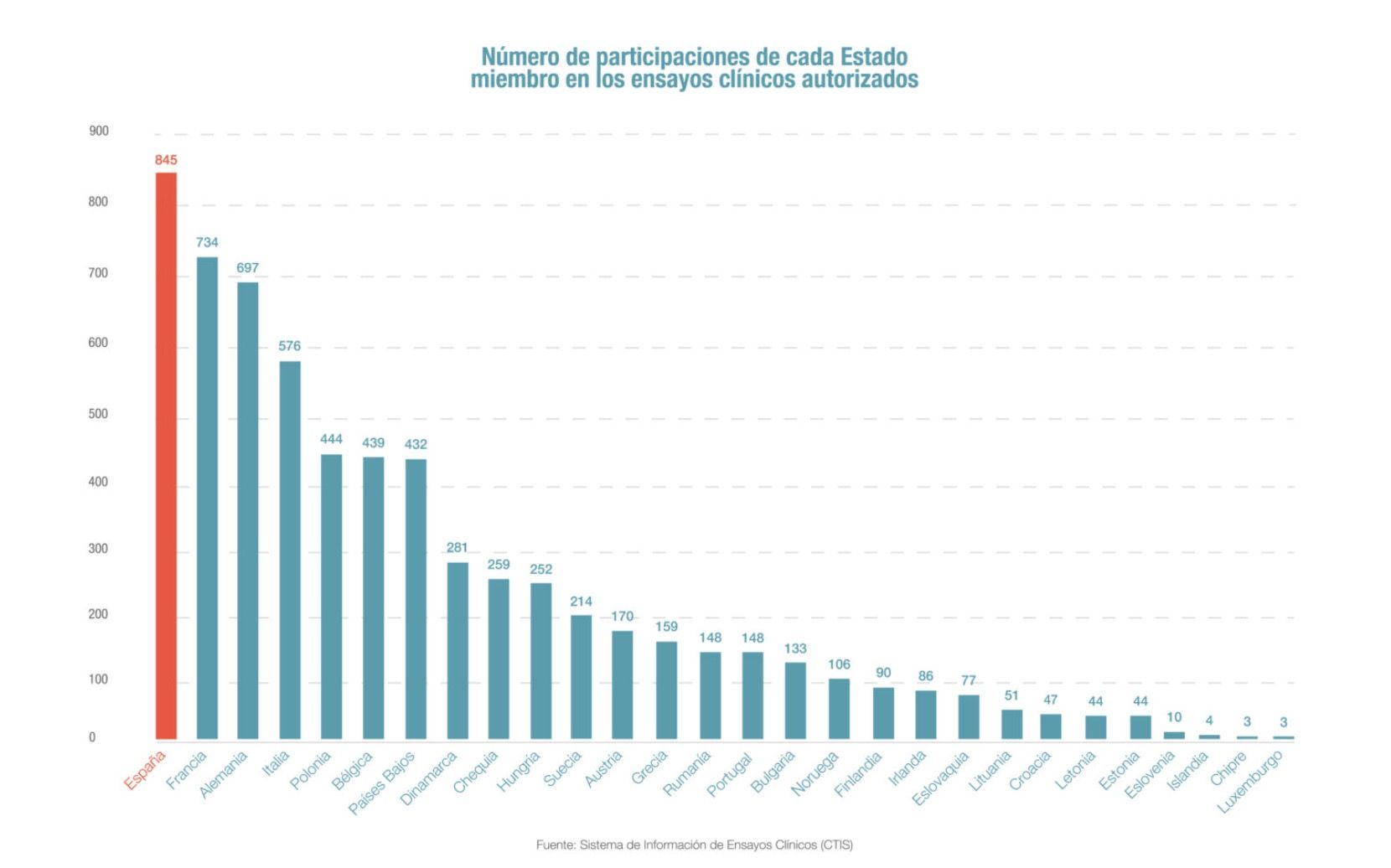
La AEMPS llama a no perder el liderazgo español en ensayos clínicos
Por su parte, la directora de la Agencia Española de Medicamentos y Productos Sanitarios (AEMPS), María Jesús Lamas, ha advertido en el reciente V Simposio del Observatorio de la Sanidad sobre la necesidad de cuidar el liderazgo mundial de España en la participación de ensayos clínicos ya que, con el nuevo Reglamento de Ensayos clínicos de 2022, "se permite agilizar e incrementar el número de ensayos multinacionales", lo que podría poner en peligro ese liderazgo nacional.
"España ha sido líder mundial, normalmente número dos después de Estados Unidos, en participación en ensayos clínicos. No únicamente como alguien que aporta de forma pasiva a pacientes, pero también formando parte del diseño de los ensayos y de la estrategia de la investigación clínica de estos medicamentos. Pero el reglamento de ensayos clínicos que entró en aplicación en enero del 2022 ha cambiado el escenario", ha señalado Lamas durante su participación en el simposio. Y es que de los 1.944 ensayos clínicos autorizados en la Unión Europea a través del nuevo Sistema Europeo de Información, los centros españoles participaron en 845, un 43% del total, según publica FarmaIndustria.

